El virus de la fiebre amarilla es el agente causal de una de las enfermedades infecciosas cuya importancia histórica, financiera y médica ha sido bien documentada, como lo demuestra la mortandad de los colonos en las campañas en África, el fracaso de los primeros intentos de construir el canal de Panamá y las epidemias que diezmaron la población de diferentes ciudades. En 1938, el científico Max Theiler desarrolló una vacuna efectiva que actualmente continúa utilizándose.
El virus de la fiebre amarilla se originó en África y llegó a América durante la era del comercio de esclavos, con la primera epidemia reportada en Yucatán en 1648. En el siglo XVIII hubo grandes epidemias de fiebre amarilla, entre agosto y noviembre de 1793 la enfermedad mató en Filadelfia aproximadamente al 10 % de la población. A fines del siglo XIX, la fiebre amarilla era una plaga conocida y temida del hemisferio occidental y las regiones costeras de África Occidental, para la cual no se conocía la causa ni el tratamiento efectivo. En 1871 ocurrió una de las mayores epidemias en la historia de Buenos Aires, se estima que en pocos meses causó la muerte del 8 % de la población [recuadro 1]. Asimismo, el mayor reto que enfrentó la construcción del canal de Panamá, que se inició en 1881, fueron las epidemias principalmente de malaria y fiebre amarilla [recuadro 2].
A fines del siglo XIX, tras la identificación del virus del mosaico de la planta de tabaco (primer virus identificado en la historia), empezaron a descubrirse virus en animales y humanos. El primer virus humano identificado fue el de la fiebre amarilla, en Cuba, en 1901. El médico cubano Carlos Finlay había postulado en la V Conferencia Sanitaria Internacional, celebrada en Washington en 1881, la teoría metaxénica del contagio de enfermedades o del vector biológico para explicar la transmisión de la fiebre amarilla y, posteriormente, una comisión especial creada por el Ejército de Estados Unidos (que ocupó Cuba hasta 1902) logró determinar que el origen del mal era un “agente filtrable”.
En junio de 1927, la sangre de Asibi, un joven de 28 años nacido en Ghana que padecía una enfermedad febril fue inyectada en un Macacus rhesus y, de este modo, se logró por primera vez un modelo animal para el estudio del virus. El principal desafío entonces era obtener una cepa atenuada del virus, que perdiera la virulencia (propiedades viscerotrópicas y neurotrópicas), pero conservara su capacidad para replicarse e inducir una respuesta inmune.
En 1930, el médico Max Theiler [Figura 1], nacido en 1899 en Pretoria, Sudáfrica, se encontraba en ese entonces trabajando en el Departamento de Medicina Tropical de la Escuela de Medicina de Harvard cuando identificó un modelo animal más conveniente que el Macacus rhesus, al demostrar que los ratones eran susceptibles a la inoculación intracerebral del virus. Durante su labor experimental Theiler contrajo fiebre amarilla, pero afortunadamente para la posteridad fue un caso leve. Para enfatizar la naturaleza peligrosa del trabajo relacionado con el virus de la fiebre amarilla, la División de Salud Internacional informó en 1931 sobre 32 casos adquiridos en ocho laboratorios con cinco fallecidos.
En 1932, Theiler y Eugen Haagen, que conocían el método de Pasteur para atenuar el virus de la rabia en tejido nervioso heterólogo, lograron cultivar el virus de la fiebre amarilla en tejido embrionario de ratón y pollo. Más importante aún, luego de múltiples pasajes, la cepa obtenida mostraba una significativa reducción del viscerotropismo (disminución del daño hepático y la enfermedad sistémica). Sin embargo, presentaba un incremento del neurotropismo.
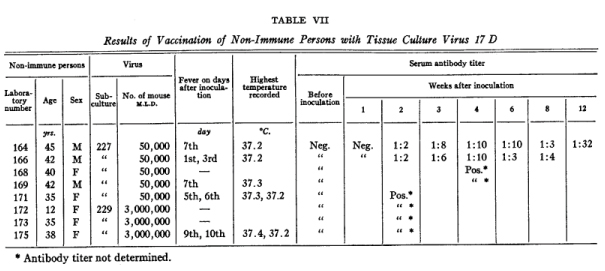
El inconveniente fue superado cuando Theillery colaboradores tuvieron la original ocurrencia de extirpar el tejido nervioso de los embriones de pollo antes de realizar los cultivos. Inicialmente realizaron 17 pasajes en tejido embrionario de ratón, posteriormente se cultivó hasta el pase 58 en tejido de pollo a partir de huevos embrionados y luego, hasta el pase 114, en tejido de pollo desnervado. El virus obtenido se inyectó intracerebralmente en monos, el cual mostraba una marcada reducción tanto en el viscerotropismo como en el neurotropismo. Finalmente, el virus se siguió subcultivando hasta el pasaje 229 y se utilizó para inmunizar a ocho voluntarios humanos quienes desarrollaron inmunidad protectiva a las 2 semanas posvacunación sin evidenciar reacciones adversas severas o graves [Figura 2]. La primera prueba de campo con la nueva vacuna se llevó a cabo en Brasil en 1938 y en los siguientes 80 años, y más de 850 millones de dosis aplicadas, la vacuna ha demostrado ser notablemente segura y eficaz.
En 1951, se le otorgó a Max Theiler el Premio Nobel de Fisiología o Medicina por sus descubrimientos sobre la fiebre amarilla y cómo combatirla. Este fue el primero y hasta ahora único Premio Nobel otorgado por el desarrollo de una vacuna contra un virus.
En la actualidad, la vacuna todavía se produce utilizando los métodos originales: se realizan pasajes del virus en tejido de pollo a partir de huevos embrionados y se almacena como un homogeneizado congelado. Se recomienda su aplicación para personas de 9 meses de edad o mayores que viajan o viven en áreas de riesgo de contraer la infección. En la Argentina, el Calendario Nacional de Vacunación programa la vacunación contra la fiebre amarilla solo para los residentes de las provincias de Misiones, Corrientes, Formosa y algunos departamentos de Chaco, Salta y Jujuy. El esquema consiste en una dosis entre los 12 y los 18 meses de edad y un refuerzo a los 11 años de edad.
Ochenta años más tarde, en 2016, se aprobaba la vacuna contra el dengue. Esta es una vacuna quimérica tetravalente atenuada en el que dos genes (prM y E) de la cepa vacunal de fiebre amarilla desarrollada por Max Theiler han sido reemplazados por los genes correspondientes de DENV-1, 2, 3 o 4, pero esta es otra historia…

EPIDEMIA DE FIEBRE AMARILLA EN BUENOS AIRES
En 1871, cuando la Argentina se encontraba bajo la presidencia de Domingo Faustino Sarmiento, ocurrió una de las mayores epidemias en la historia de Buenos Aires, se estima que entre enero y mayo la epidemia causó la muerte de 13.500 y 14.500 habitantes de la ciudad (8 % de la población).
Se cree que la epidemia habría provenido de Asunción del Paraguay, portada por los soldados argentinos que regresaban de la Guerra de la Triple Alianza (1864-1870); ya que previamente se había propagado en la ciudad de Corrientes en 1870 (2.000 fallecidos en 6 meses). En su peor momento, la población porteña se redujo a menos de la tercera parte, debido al éxodo de quienes abandonaron la ciudad para intentar escapar del flagelo.
El cementerio del Sur, situado donde actualmente se encuentra el parque Ameghino, vio rápidamente colmada su capacidad. El gobierno municipal adquirió entonces siete hectáreas en las afueras de la ciudad en la Chacarita de los Colegiales y creó allí el Cementerio del Oeste. Quince años más tarde, este se trasladaría a pocos metros de allí, al actual Cementerio de la Chacarita.

FIEBRE AMARILLA Y EL CANAL DE PANAMÁ
La idea de crear un paso de agua a través del istmo de Panamá para unir los océanos Atlántico y Pacífico se remonta al menos al año 1500: después de que el explorador Vasco Núñez de Balboa se dio cuenta de que una estrecha franja de tierra separaba los dos océanos, el rey Carlos I de España llamó a su gobernador regional para inspeccionar una ruta a lo largo del río Chagres.
En 1534, Carlos V de España ordenó el primer estudio sobre una propuesta para una ruta a través del istmo de Panamá. Más de tres siglos transcurrieron antes de que se comenzara la construcción. Francia fue finalmente el primer país en intentar la tarea. La obra se inició en 1880, dirigida por el Conde Ferdinand de Lesseps, el constructor del canal de Suez en Egipto. A diferencia del árido desierto del istmo de Suez, Panamá era una selva tropical, con lluvias diluviales, calor, humedad y enfermedades tropicales.
Las fiebres tropicales, en particular la fiebre amarilla y la malaria, diezmaron las filas de los franceses, de las decenas de miles de trabajadores que construyeron el canal francés, más del 85 % fueron hospitalizados y 22.000 murieron principalmente a causa de la fiebre amarilla. Las víctimas eran sepultadas en el cementerio de Ancón. Finalmente, en 1888 los franceses abandonaron el proyecto que finalmente fue llevado a cabo por los estadounidenses e inaugurado en 1914.
En su manuscrito “The inside history of a great medical discovery”, Aristides Agramonte de la Universidad de Cuba en 1915 sostuvo que la construcción del canal de Panamá fue posible porque se demostró que la fiebre amarilla, al igual que la malaria, solo podía transmitirse por la picadura de mosquitos infectados y, en consecuencia, se crearon brigadas de fumigación para desinfestar de mosquitos la región.



https://www.usmcu.edu/Portals/218/LLI/MLD/How%20to%20Eradicate%20a%20Scourge.pdf?ver=2018-11-27-160223-62
FIEBRE AMARILLA
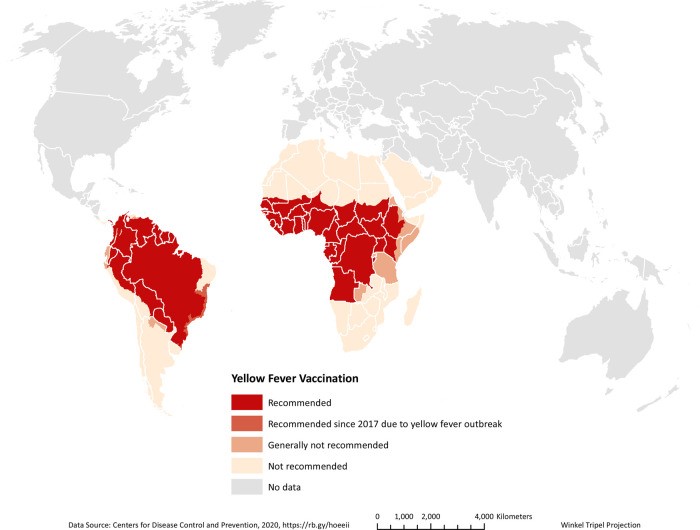
La infección por el virus de la fiebre amarilla puede causar desde una enfermedad febril leve sin ictericia hasta insuficiencia hepatorrenal y muerte. Actualmente, se estima que causa 200.000 casos de enfermedad y 30.000 muertes cada año (el 90 % ocurre en África). Asimismo, el 20 al 50 % de las personas infectadas que desarrollan una enfermedad grave mueren.
Los brotes de fiebre amarilla resurgen del bosque cada 7 u 8 años. Entre 2016–2019, el virus se propagó en Brasil en áreas sin antecedentes de inmunidad adquirida o cobertura de vacunación obligatoria, causando 2166 casos confirmados y 751 muertes. De manera similar, un brote simultáneo en Angola y la República Democrática del Congo resultó en 884 casos confirmados y 381 muertes, exportando casos hasta China.
En nuestro país los últimos casos detectados datan de 2008, cuando el Ministerio de Salud de la Argentina confirmó 5 casos, incluyendo 1 muerte en la provincia de Misiones.
ATENUACIÓN
La atenuación de un virus es consecuencia del proceso de adaptación de este al hospedador. La adaptación es la resultante de mutaciones en el genoma viral y, si bien se mantiene la capacidad replicativa, una vez adaptado a un hospedador diferente al original es posible que reintroducido en el hospedador original la virulencia se haya suprimido.
En 1885 Pasteur descubrió que la virulencia del virus de la rabia, mantenida por el pasaje intracraneal en serie en perros, disminuía cuando el material infectado se inyectaba en diferentes especies. Comenzando con una cepa altamente virulenta (“salvaje”) pasada en serie muchas veces en conejos obtuvo una cepa atenuada que, al inyectarla nuevamente en perros, no solo no les causaba enfermedad, sino que además los protegía con éxito frente a la exposición al “virus salvaje”. El 6 de julio de 1885, a regañadientes, ya que Pasteur no era un médico licenciado y podría haber sido procesado por hacerlo, Pasteur empleó, en presencia de dos médicos locales, la cepa atenuada para tratar a Joseph Meister, un niño de 9 años, que había sido mordido gravemente por el perro rabioso de un vecino. Joseph Meister recibió un total de 13 inoculaciones durante un período de 11 días y sobrevivió con buena salud.
Max Theillery y colaboradores obtuvieron la cepa atenuada (17D) luego de realizar, durante más de tres años, 229 pasajes sucesivos del virus salvaje en tejidos heterólogos (embriones de ratón, de pollo y de pollo denervado). La cepa vacunal era no virulenta e inducía una respuesta inmune protectiva sin evidenciar reacciones adversas severas o graves. Cincuenta años después de su desarrollo se determinó que la diferencia entre la cepa salvaje y la cepa atenuada (17D) eran mutaciones en solo 68 de los 10.862 nucleótidos que componen el genoma viral (Hahn CS et al. Comparison of the virulent Asibi strain of yellow fever virus with the 17D vaccine strain derived from it. Proc Natl Acad Sci USA, 1987).
Diego Flichman es doctor de la UBA, profesor adjunto de la Cátedra de Virología de la Facultad de Farmacia y Bioquímica e investigador independiente del CONICET.
Bibliografía
Theiler M & Smith HH. The effect of prolonged cultivation in vitro upon the pathogenicity of yellow fever virus. Journal of Experimental Medicine 1937.
Theiler M & Smith HH. The use of yellow fever virus modified by in vitro cultivation for human immunization. Journal of Experimental Medicine 1937.








