Uno de los grandes desafíos asociados a la producción de medicamentos a partir de compuestos naturales radica en desarrollar plataformas de producción de biomoléculas para satisfacer la demanda de la industria farmacéutica. La biotecnología es una disciplina que aporta herramientas útiles para lograr este objetivo.
Desde el inicio de los tiempos, las plantas han sido utilizadas por el hombre para tratar distintas patologías y afecciones. Por acción de su propio metabolismo, ciertas especies vegetales producen compuestos químicos que tienen efectos farmacológicos sobre los seres vivos. En algunos casos, las plantas con acción medicinal se utilizan directamente en forma de tisanas o decocciones, o bien, se elaboran preparaciones farmacéuticas con sus extractos. En otros casos, los compuestos con actividad farmacológica son aislados desde la fuente vegetal e incluidos en medicamentos como principios activos.
Entre los compuestos más importantes aislados a partir de plantas se encuentran los medicamentos antimaláricos quinina y artemisinina, obtenidos de la corteza de diferentes especies de quina (Cinchona spp.) y a partir de Artemisia annua, especie empleada en la medicina china para el tratamiento de la fiebre, respectivamente. La utilización de Digitalis purpurea para el tratamiento de enfermedades cardíacas, condujo al aislamiento de la digoxina.
Otros ejemplos lo constituyen la morfina, analgésico aislado en 1816 de Papaver somniferum; la reserpina, agente antihipertensivo de Rauwolfia serpentina; la efedrina aislada por primera vez de Ephedra sinica en 1887; y la tubocurarina, relajante muscular aislado de especies de Chondrodendron. Los alcaloides atropina y pilocarpina, aislados de Atropa belladona y especies de Pilocarpus, utilizados como antiespasmódico y para el tratamiento del glaucoma, respectivamente, y los anticancerígenos vinblastinay vincristinade Catharanthus roseus constituyen otros ejemplos de moléculas obtenidas de plantas y que son utilizadas en la actualidad.
Una problemática que se presenta en la obtención de principios activos a partir de plantas es que, al ser extraídos de fuentes naturales, el rendimiento en la producción de estas moléculas activas resulta a menudo insuficiente. Además, se pone en riesgo la conservación de las plantas al explotar la fuente natural, a la vez que la cantidad de principios activos sintetizados se ve condicionada por factores climáticos y ambientales. Finalmente, cabe destacar que la síntesis química de compuestos activos de origen vegetal en la mayoría de los casos es económicamente inviable dada la complejidad estructural de este tipo de moléculas.
Entonces, uno de los grandes desafíos asociados a la producción de medicamentos a partir de compuestos naturales radica en desarrollar plataformas de producción de biomoléculas para satisfacer la demanda de la industria farmacéutica. La biotecnología es una disciplina que aporta herramientas útiles para lograr este objetivo.
La biotecnología es una ciencia multidisciplinaria que combina conocimientos del campo de la biología, la química, la genética y la ingeniería, que permite desarrollar procesos utilizando organismos vivos o partes de ellos para obtener productos o servicios. Existen diferentes áreas de aplicación, tales como la biotecnología aplicada a la salud humana y animal, la biotecnología industrial, la biotecnología ambiental y la biotecnología vegetal. Esta última rama abarca, entre otros, el mejoramiento genético de plantas y la producción a gran escala de cultivos vegetales in vitro.
El cultivo vegetal in vitro hace referencia al cultivo de células u órganos de una especie vegetal determinada, en condiciones controladas de temperatura y luz, en un medio de cultivo que satisfaga sus requerimientos nutricionales y en ausencia de patógenos. Esta alternativa de cultivo vegetal y producción de compuestos de interés se fundamenta en dos características que presentan las células vegetales: la plasticidad para adaptarse a cambios en el medio ambiente, y la capacidad de crecer y regenerar un individuo completo (totipotencialidad).
En el laboratorio, es posible obtener diferentes tipos de cultivos vegetales in vitro a partir de una porción de tejido vegetal, empleando distintos reguladores de crecimiento (también llamados hormonas vegetales). Los más comúnmente empleados son auxinas y citoquininas, que promueven diferentes cambios morfológicos y metabólicos en las células.
Según la concentración y la combinación de auxinas y citoquininas agregadas al medio de cultivo, pueden obtenerse células desdiferenciadas capaces de crecer en medio de cultivo sólido (cultivo de callos) o en medio líquido (suspensiones celulares), cultivos de tallos, cultivos de raíces adventicias. Incluso, mediante el cultivo in vitro, pueden propagarse individuos completos (micropropagación), que permite obtener una gran cantidad de individuos genéticamente idénticos (clones), en cortos períodos y en espacios reducidos.
Además, por infección del tejido vegetal con Agrobacterium rhizogenes, pueden obtenerse raíces transformadas que crecen indefinidamente sin el agregado de reguladores de crecimiento tanto en medio de cultivo sólido como en medio líquido.
La posibilidad de establecer cultivos in vitro de una planta con propiedades medicinales presenta múltiples ventajas. Por un lado, permite la producción continua y homogénea del compuesto de interés, ya que esta no se ve afectada por factores climáticos ni por el riesgo de pérdida por potenciales patógenos. Por otra parte, esta estrategia es amigable con el medio ambiente ya que evita la explotación de la especie productora y la protege frente a un potencial riesgo de extinción.
Además, las condiciones de cultivo controladas permiten la producción con calidad acorde con las normas de producción de medicamentos. Asimismo, la manipulación genética de la especie productora para favorecer la acumulación del compuesto de interés se realiza sobre plantas cultivadas in vitro.
Finalmente, en este tipo de cultivos pueden aplicarse distintos estímulos capaces de aumentar la producción del compuesto de interés. Entre ellos, pueden mencionarse: componentes celulares de patógeno o que tienen semejanza estructural con ellos (extractos fúngicos o bacterianos, quitosano), compuestos que participan en las vías de señalización celular vegetal (ácido salicílico, metiljasmonato), precursores de la vía de síntesis del compuesto de interés o inhibidores de vías que compiten por intermediarios de la ruta biosintética.
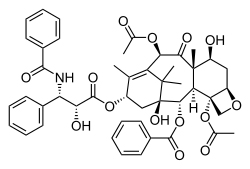
Un ejemplo de la aplicación de la biotecnología para la obtención de principios activos de origen vegetal lo constituye la producción de paclitaxel. El paclitaxel es un terpeno (taxano) obtenido a partir de la corteza de árboles pertenecientes al género Taxus.Este compuesto es uno de los fármacos utilizados en la quimioterapia de diferentes tipos de cáncer, tales como cáncer de mama, ovario, próstata y pulmón, entre otros.
La producción de paclitaxel se realiza a partir de suspensiones de células vegetales cultivadas en biorreactores. El incremento del rendimiento en la producción de este terpeno a través de esta tecnología ha sido tan importante que en la actualidad existen empresas que producen y exportan el principio activo obtenido a partir de suspensiones de células vegetales de Taxus chinensis.
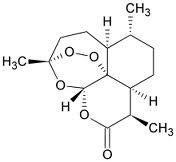
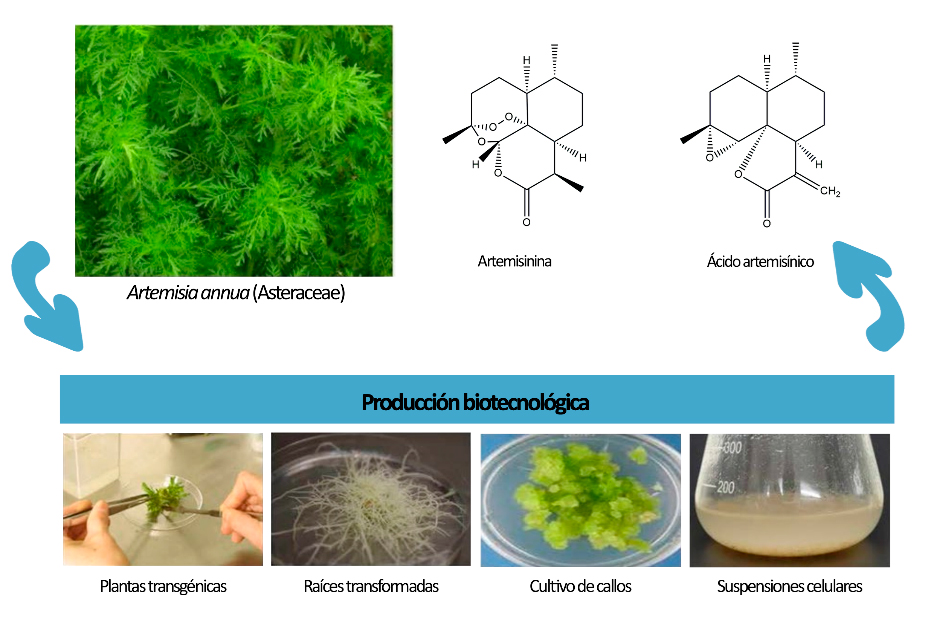
Otro ejemplo de la aplicación de la biotecnología en la producción de medicamentos a base de plantas lo constituye la artemisinina. La artemisinina es un compuesto terpénico (lactona sesquiterpénica), aislado a partir de la hierba medicinal china Artemisia annua (Asteraceae), que se utiliza como agente antimalárico. La malaria es una enfermedad que puede ser mortal y que afecta a las poblaciones más pobres y en vías de desarrollo. A partir del compuesto natural se han sintetizado derivados con mayor actividad y biodisponibilidad, como el artemeter, arteeter y artesunato. La terapia combinada de otros antimaláricos junto con derivados de artemisinina es actualmente utilizada en el tratamiento de la malaria y avalada por la Organización Mundial de la Salud.
La artemisinina es sintetizada en las hojas de A. annua, específicamente en los pelos glandulares. Debido a que la planta tiene un contenido relativamente bajo de artemisinina (0,5 % referido a la planta seca), y su síntesis no es viable económicamente, se extrae de la planta y luego se derivatiza. Para aumentar el rendimiento se utiliza como precursor el ácido artemisínico, que se encuentra presente en mayores cantidades en esta especie, y luego se convierte químicamente en artemisinina y sus derivados.
Numerosos grupos de investigación han abordado la producción de ácido artemisínico y artemisinina en cultivos in vitro de A. annua. Se han establecido cultivos de suspensiones celulares, de callos, de tallos y de raíces transformadas. Como se mencionó, además se han aplicado diversas estrategias con el fin de favorecer la acumulación de los compuestos de interés. Entre ellos, se ha estimulado la producción con el agregado de quitosano, metiljasmonato y de compuestos que son precursores de biosíntesis de artemisinina.
Otra estrategia que fue evaluada en cultivos in vitro consistió en obtener plantas transgénicas de A. annua. En este sentido, se ha buscado aumentar los niveles de acumulación de artemisinina mediante la sobreexpresión de genes relacionados con su biosíntesis, ya sean genes que codifican enzimas involucradas en la ruta biosintética, genes que codifican proteínas que regulan a los anteriores, y otros. Por ejemplo, un grupo de investigadores ha obtenido plantas de A. annua genéticamente modificadas que producen un alto contenido de artemisinina. El gen sobre el que han trabajado, AaMYB1, se encuentra implicado en la formación de pelos (tricomas) vegetales y en la síntesis de terpenos, como la artemisinina.
A partir de cultivos de Artemisia annua se ha trabajado en mejorar el rendimiento de artemisinina y se ha llegado a un 2 %.
OTRAS ESTRATEGIAS BIOTECNOLÓGICAS DE PRODUCCIÓN DE ARTEMISININA
En los últimos años se han desarrollado diferentes técnicas para aumentar el rendimiento de ácido artemisínico. En este sentido, y con implicancia de la biotecnología, varios grupos de investigación han trabajado en la transferencia de los genes de las enzimas básicas de la ruta metabólica del ácido artemisínico de A. annua al genoma del cloroplasto y de la mitocondria de las plantas de tabaco. El tabaco es un cultivo de alta biomasa. Así se han logrado obtener niveles mayores de ácido artemisínico en sus hojas.
Otra metodología para la producción de artemisinina se basa en la producción microbiana de ácido artemisínico. En este caso, se han logrado aislar los genes involucrados en la biosíntesis de artemisinina y se han introducido, por técnicas de ingeniería genética, en la levadura Saccharomyces cerevisiae. El resultado es la producción de ácido artemisínico en la levadura y su posterior derivatización química en artemisinina.
Estos estudios muestran los aportes de la biotecnología en el cultivo de especies vegetales de interés farmacéutico y en la reducción de los costos de producción de medicamentos a partir de plantas.
Laura C. Laurella. Instituto de Química y Metabolismo del Fármaco (IQUIMEFA) (UBA-CONICET) y Cátedra de Farmacognosia – Facultad de Farmacia y Bioquímica, Universidad de Buenos Aires.
Orlando G. Elso. Cátedra de Farmacognosia – Facultad de Farmacia y Bioquímica, Universidad de Buenos Aires.
Valeria P. Sülsen. Instituto de Química y Metabolismo del Fármaco (IQUIMEFA) (UBA-CONICET) y Cátedra de Farmacognosia – Facultad de Farmacia y Bioquímica, Universidad de Buenos Aires.
María Perassolo. Instituto de Nanobiotecnología (NANOBIOTEC) (UBA-CONICET) y Cátedra de Biotecnología– Facultad de Farmacia y Bioquímica, Universidad de Buenos Aires.
Julián Rodríguez Talou. Instituto de Nanobiotecnología (NANOBIOTEC) (UBA-CONICET) y Cátedra de Biotecnología – Facultad de Farmacia y Bioquímica, Universidad de Buenos Aires.