La inhalación de partículas de contaminación ambiental agrava el infarto agudo de miocardio a través de un desbalance del sistema inmune, provocado por la liberación de TNF-α al torrente sanguíneo por parte de los macrófagos alveolares (adaptado de Marchini y col., Basic Research in Cardiology 2016;111(4):44).
La Organización Mundial de la Salud estima que la inhalación de aire contaminado causa unas 7 millones de muertes por año. Los niños, ancianos y personas de bajo nivel socioeconómico o con enfermedades cardiorrespiratorias preexistentes representan los principales grupos de riesgo. A pesar de que el pulmón es el primer órgano en contacto con el aire que respiramos, las principales causas de muerte reportadas se deben a las enfermedades del sistema circulatorio, como el accidente cerebrovascular y el infarto agudo de miocardio. En esta nota se exploran los caminos por los cuales la exposición a la contaminación ambiental, y en especial al material particulado, que es invisible al ojo humano, produce efectos perjudiciales a la salud cardiovascular de los habitantes de las grandes ciudades.
La contaminación ambiental se puede definir como la presencia en la atmósfera de sustancias capaces de producir daño tanto a la vida como a los materiales y estructuras creados por el hombre. A pesar de que en el aire que respiramos se pueden encontrar numerosos compuestos con potenciales efectos perjudiciales sobre la salud, diversos estudios indican que el principal responsable es el material particulado (MP), especialmente el que proviene del uso de combustibles fósiles por el tráfico vehicular y de diversas actividades industriales. Este MP consiste de partículas sólidas de un tamaño menor a 10 micrómetros, es decir, unas 5 veces menos que un cabello. Son completamente invisibles para el ojo humano, sin embargo, son lo suficientemente pequeñas como para ingresar libremente al sistema respiratorio y llegar hasta los alvéolos pulmonares donde ejercen su efecto tóxico.
Se ha demostrado que el daño que produce el MP en el pulmón es causado por un proceso inflamatorio local y alteraciones en el metabolismo del oxígeno. Sin embargo, hasta ahora, no se ha establecido claramente cómo se relaciona este escenario con efectos perjudiciales sobre el corazón, particularmente en cuanto a la incidencia y la progresión de la principal enfermedad asociada a la exposición al MP, es decir, el infarto agudo de miocardio (IAM).Trabajos previos mostraron que la presencia de metales de transición como constituyentes del MP favorecen la activación del sistema inmune en el pulmón, dañando el tejido a través de una producción exacerbada de compuestos oxidantes derivados del oxígeno. Debido a su relevancia como contaminante ambiental y a su composición química particular (caracterizada por contener altas cantidades de hierro, níquel y vanadio) las partículas ROFA (del inglés, Residual Oil Fly Ash) han sido especialmente útiles para entender los efectos tóxicos del MP, principalmente a nivel del sistema respiratorio.
Para estudiar los efectos de la contaminación ambiental sobre el corazón utilizamos un modelo de exposición al MP mediante la administración intranasal de partículas ROFA en ratones. Los primeros resultados obtenidos mediante este procedimiento mostraron una marcada depresión del metabolismo cardíaco debido a alteraciones en la función de la mitocondria, la principal organela subcelular encargada de producir la energía necesaria para el correcto funcionamiento de las células. Este aporte deficiente de energía al corazón provocó una menor capacidad para bombear la sangre adecuadamente en los animales expuestos al MP. La liberación de distintos mediadores inflamatorios desde el pulmón, como el factor de necrosis tumoral alfa (TNF-α, del inglés Tumor Necrosis Factor α), parecerían ser los responsables de los efectos observados sobre el corazón. De hecho, la administración de una droga que bloquea específicamente la actividad biológica del TNF-α (conocida como infliximab, actualmente utilizada para el tratamiento de la artritis reumatoide y otras enfermedades autoinmunes) previno las alteraciones metabólicas observadas en el corazón y mejoró la capacidad contráctil cardíaca en los animales expuestos al MP.
Por otro lado, hemos visto que los macrófagos alveolares, un tipo celular del sistema inmune residente en el pulmón y especializado en fagocitar todo tipo de sustancias extrañas que lleguen a este órgano, son los principales productores de TNF-α luego de la inhalación de MP. En respuesta a esta liberación de TNF-α, otras células del sistema inmune, como los monocitos y los neutrófilos, se activan y comienzan a poblar el pulmón, lo que amplifica la respuesta inflamatoria y el daño al tejido.
Al mismo tiempo, la capa de células que recubre los vasos sanguíneos, el endotelio, también se activa en respuesta al TNF-α liberado por los macrófagos alveolares. Este proceso implica, entre otras cosas, la expresión de moléculas de adhesión sobre la superficie de las células, lo que permite a monocitos y neutrófilos rodar sobre el endotelio, adherirse, y migrar hacia la zona lesionada.
En un IAM se produce un daño del tejido cardíaco por obstrucción de alguno de los vasos sanguíneos que lo irrigan, conocidos como arterias coronarias. La extensión del área afectada y, principalmente, su cicatrización, dependerán de un correcto funcionamiento del sistema inmune. Por un lado, para limpiar el tejido dañado y, por el otro, para repararlo adecuadamente y permitir que el corazón recupere su función normal. Esta activación exacerbada del sistema inmune producida por la exposición al MP, que es orquestada por los macrófagos alveolares y mediada por el TNF-α, parecería alterar este delicado balance. De hecho, los animales expuestos a ROFA presentaron una mayor área de infarto luego de sufrir un IAM. Esta secuencia de procesos podría explicar, al menos en parte, la mayor incidencia y el peor pronóstico del IAM en residentes de áreas contaminadas.
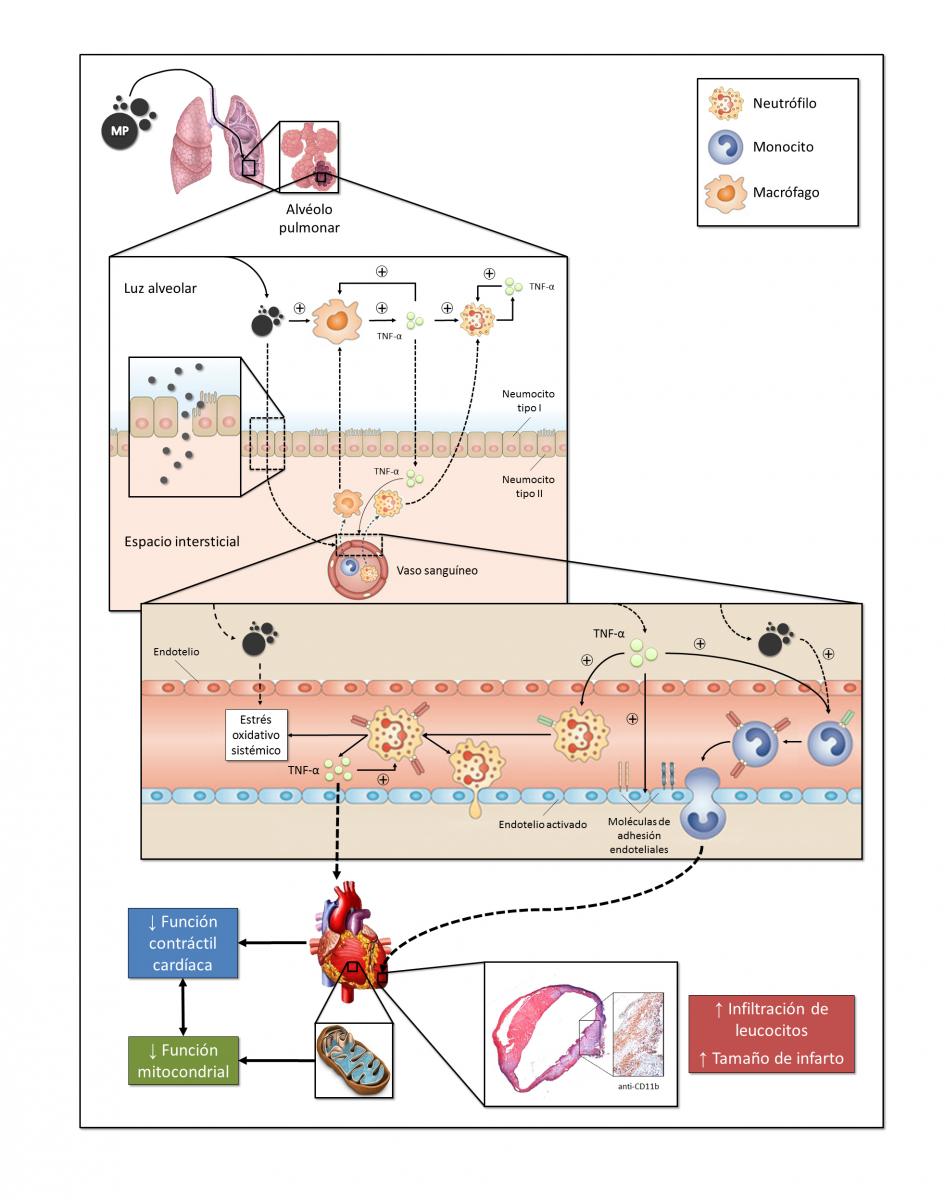
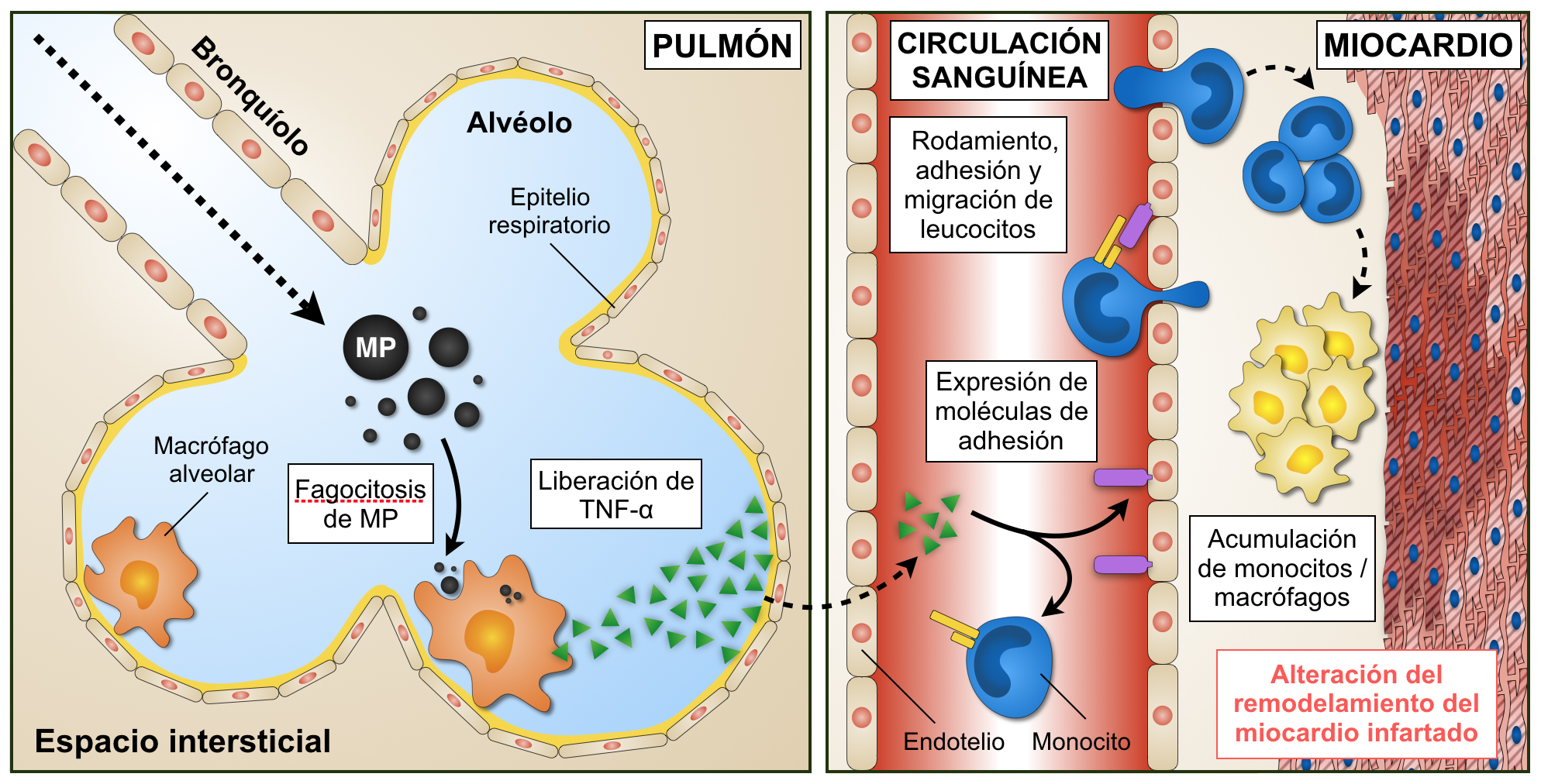
Modelo de los mecanismos disparados por la exposición al MP
La inflamación local promovida por la presencia de MP en el pulmón es orquestada por los macrófagos alveolares y el TNF-α. La liberación de estos mediadores inflamatorios desde el pulmón hacia la circulación sanguínea afecta la capacidad contráctil del corazón por alteraciones en la función mitocondrial. Por otro lado, el desbalance del sistema inmune que provoca la inhalación de MP afecta negativamente la recuperación del tejido cardíaco luego de sufrir un IAM.
La relevancia de nuestro estudio radica, entonces, en ayudar a entender los mecanismos a través de los cuales el pulmón y el corazón pueden desarrollar una respuesta integrada al respirar aire contaminado, y contribuyen a la comprensión del aumento de la morbilidad y mortalidad cardiovascular en las grandes ciudades. De esta manera, hemos podido identificar potenciales blancos terapéuticos que permitirán enfocar los esfuerzos para enfrentar esta problemática, así como desarrollar estrategias adecuadas para frenar su avance.
Glosario
Material particulado (PM): cuerpos sólidos microscópicos dispersos en la atmósfera, generados a partir de alguna actividad antropogénica o natural, que pueden ser tóxicos para la salud de las personas.
Sistema inmune: conjunto de células, estructuras y procesos biológicos le permiten al organismo defenderse frente a agresiones externas, ya sean de naturaleza biológica (virus, bacterias, parásitos) o fisicoquímica (como agentes contaminantes o radiaciones), e internas (por ejemplo, células cancerosas).

Dr. Timoteo Marchini
Tesis doctoral difundida:
“Exposición aguda a partículas de contaminación ambiental: Función cardíaca, estrés oxidativo y mecanismos de respuesta inflamatoria sistémica”.
Tesis doctoral. Facultad de Farmacia y Bioquímica. Universidad de Buenos Aires, 2015.
Timoteo Marchini trabajó bajo la dirección del profesor doctor Pablo Evelson en el Instituto de Bioquímica y Medicina Molecular (UBA-CONICET) subsede Química General e Inorgánica de la Facultad de Farmacia y Bioquímica de la Universidad de Buenos Aires. Colaboraron en el desarrollo de este proyecto la doctora Verónica D'Annunzio y el profesor doctor Ricardo Gelpi del Departamento de Fisiopatología de la Facultad de Medicina de la Universidad de Buenos Aires; la doctora Mariela Paz y el doctor Daniel González Maglio del Instituto de Estudios de la Inmunidad Humoral (UBA-CONICET) de la Facultad de Farmacia y Bioquímica de la Universidad de Buenos Aires; y los doctores Dennis Wolf e Ingo Hilgendorf, y el profesor doctor Andreas Zirlik del Departamento de Cardiología y Angiología de la Universidad de Friburgo, Alemania. La tesis, defendida el 30 de marzo de 2015, mereció la calificación de 10, Sobresaliente, Summa cum laude, y fue premiada por la Asociación Química Argentina con el premio bienal “Dr. Pedro N. Arata 2016” a la mejor tesis de doctorado en el área de Toxicología.










Comentarios (1)
Dejar un comentario